
近日,四川省肿瘤医院放疗科王奇峰团队在Nature子刊《Nature Communications》(IF: 14.7,中科院1区Top)发表了一项题为“Toripalimab plus chemotherapy and radiotherapy for treatment-naive advanced esophageal squamous cell carcinoma: A single-arm phase 2 trial”的研究。该研究为单中心、前瞻性II期临床试验,首次证明了放疗联合化学免疫治疗作为晚期食管鳞癌一线治疗的安全性和有效性,为新的临床治疗策略提供了有力的证据支持。
食管癌是我国高发肿瘤之一,约占全球病例的50%。大部分食管癌患者在初诊时已处于局部晚期或伴有远处转移,治疗手段有限,预后较差。当前,NCCN指南推荐化疗联合免疫治疗作为晚期食管癌的一线治疗方案,但其中位无进展生存期(PFS)仅为6个月左右(5.7-7.3个月)。先前一些关于食管癌寡转移的回顾性研究表明,放疗可延长患者的PFS和总生存期(OS)。然而,在化疗联合免疫治疗基础上,在一线治疗中加入局部放疗是否能够进一步提高疗效,目前尚无前瞻性研究。基于此,王奇峰团队开展了一项单臂前瞻性研究,以评估放疗联合化学免疫治疗作为晚期食管鳞癌一线治疗的安全性和有效性。
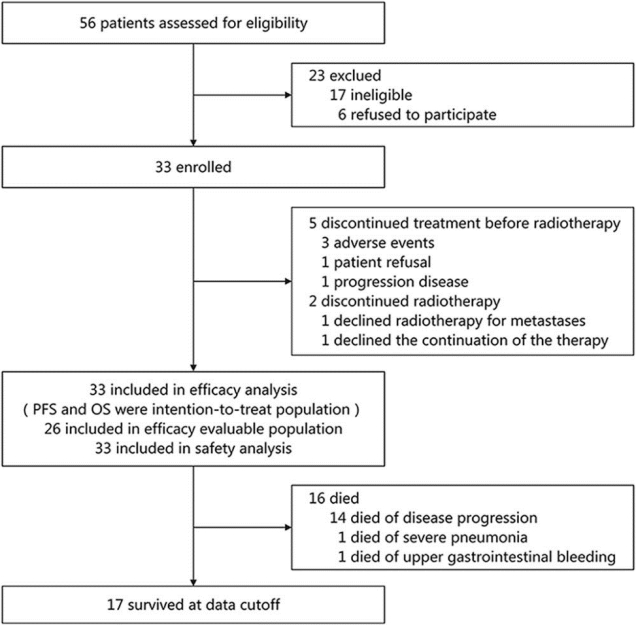
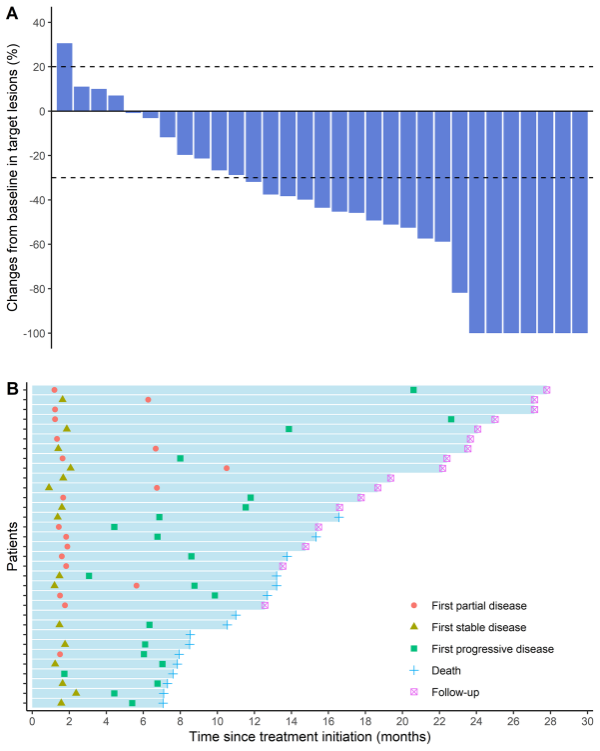
该研究历时近四年,共筛选了56名患者,其中33名患者成功入组,主要为寡转移食管鳞癌患者(27例),以及初诊不适合根治性手术或放疗的cTanyN3M0 IV期食管鳞癌患者(6例)。其中26名患者完成了食管原发病灶和所有转移病灶的放疗及4个周期的化疗联合免疫治疗。结果显示:在意向治疗(ITT)人群中(33例患者),中位随访时间为22.2个月,中位缓解持续时间(DoR)为11.5个月,中位PFS为9.8个月(较既往研究中标准化免治疗组的5.7-7.3个月显著延长),而中位OS尚未达到。最常见的不良反应为体重减轻和厌食,常见的3级或以上不良反应包括淋巴细胞减少(27/33,82%)、中性粒细胞减少(9/33,27%)和白细胞减少(8/33,24%)。整体方案安全性良好,毒副反应可控。同时,研究对生物标志物进行了探索性分析,发现肿瘤组织中CD8+ T细胞、CD11c+树突状细胞(DC)和CD68+巨噬细胞密度与治疗反应和患者预后相关。基线血清IFN-γ水平升高与治疗中IL-6水平降低及PFS延长存在显著正相关性,提示其可能作为疗效预测标志物。

本研究在晚期食管鳞癌一线化疗联合免疫治疗的基础上,针对原发灶及转移灶加入局部放疗,显著提高了临床疗效,并且安全性良好,为寡转移患者提供了一种新的治疗策略,有望为这些患者带来更长的生存期。相关研究成果入选2024年美国放射治疗年会(ASTRO)科学计划委员会的“杰出摘要奖”,在全球2000篇收录摘要中仅30篇获奖,得到了国际同行专家的认可。基于上述研究结果,我们正在开展一项多中心、随机对照III期临床试验,以进一步验证一线放疗联合化疗免疫治疗的疗效(ClinicalTrials.gov: ChiCTR2300070300)。
在院党委和院领导班子的坚强领导下,放疗科以临床需求为导向,积极开展临床研究和基础转化研究。本项目得到了放疗科首席专家郎锦义教授、李涛教授和胸外科韩泳涛教授、彭林教授的指导,由放疗科王奇峰教授团队具体负责实施。放疗科吴磊主治医生、李柏森副主任医师和万刚主治医师为论文的并列第一作者,放疗科王奇峰教授、研究所曹邦荣副教授和病理科刘洋教授为论文的共同通讯作者。同时,本研究得到了医院胸外科、病理科、检验科、影像科和研究所等多个科室的大力支持,以及天津医科大学肿瘤医院章文成教授团队的指导。
我院放疗科和胸外科是我国西部地区最大的食管癌诊疗中心,集肿瘤治疗、科研和教学于一体。每年我们治疗近1000名食管癌患者,凭借先进的医疗设备和技术,诊疗水平达到国际一流水平。在医院和科室领导的重视和支持下,我们不仅专注于高质量的临床工作,还在科研和教学方面取得了显著进展。我们的科研团队积极参与国内外的学术交流和合作,不断探索和创新。在过去几年中,我们已成功联合培养了多名博士和硕士研究生,为肿瘤学领域输送了大量高素质的人才。我们的研究团队在食管癌治疗方面取得了多项重要成果。我们开展了多项临床试验,涉及新型放化疗方法、个体化治疗方案和生物标志物研究等领域。这些研究不仅在国内外学术界引起了广泛关注,还为临床实践提供了宝贵的数据和经验。我们的目标是通过不断的创新和努力,为食管癌患者提供更好的治疗选择和生活质量,并在国际肿瘤学领域树立起新的标杆。


